實例1:
濕熱滅菌設備的溫度驗證
1溫度驗證程序規劃底子請求
濕熱滅菌的底子程序規劃底子請求源于US.FDA在上世紀70年代中期提出的,且在80年代施行的:“對于大容量注射劑GMP技能性準則”五個方面請求:
(1)在滅菌工序應能確保商品到達F0 ≥ 8;
(2)滅菌前,待實驗的容器中有**高帶菌量,污染菌應具有**強的耐熱性;
(3)每一個滅菌釜的每種裝載辦法及每種規范容器的驗證實驗均**少運用10支熱電偶進行熱散布實驗;
(4)用待實驗容器灌注粘度相類似的商品進行熱穿透實驗,找出容器中升溫**慢點的方位,**少運用10個容器,每個均參加恰當的生物指示劑并且插有熱電偶。當滅菌釜的參數現已到達熱散布實驗現已證實的可重現情況,溫度到達設定的滅菌溫度時,開端測定F0 值,直到開端冷卻止;
(5)當商品到達滅菌溫度直到開端冷卻的進程,溫度改變有必要堅持在±0.5℃以內。
2溫度驗證的功用測驗進程
由此技能規劃請求動身,演化變成如今G內廣泛選用的濕熱溫度驗證的大容量注射劑實驗辦法和實驗用具,也是溫度驗證程序規劃的底子請求。運用其作功用測驗進程及參閱設備如下:
前提: 濕熱滅菌設備的設備測驗合格,現場和共用工程外接條件完備。即通常講(DQ,IQ)現已完畢后,方位在OQ運轉承認。
2.1熱散布測驗
意圖:找出**冷點方位,查驗重現性。進程:(1)設備儀器校對;(2)熱電偶散布圖;(3)空載熱散布實驗,3次以上;(4)熱電偶刺進圖;(5)裝載(模仿出產裝載**大,**小量)熱散布實驗,各3次以上。
2.2熱穿透測驗
意圖:必定滅菌進程中被測驗各點取得無菌確保值,格外是**冷點方位的F0 值,監測查驗重現性。進程:(1)設備校對;(2)模仿出產滅菌裝載;(3)熱電偶裝載圖;(4)同品同規商品**大與**小裝載熱穿透實驗,每情況3次以上。
2.3 生物指示劑測驗
意圖: 挑戰性模仿出產或許要素形成的微生物污染程度來查驗滅菌牢靠性,對驗證規劃進行查驗。進程:(1)計劃的規劃擬定;(2)生物指示劑菌株的挑選,測定D值;(3)標定濃度和擬定樣品;(4)接種,裝載;(5)低限滅菌(每商品,每規范每種滅菌程序**少3次以上);(6)樣品的培育與辨別;(7)評估定論(數據,樣品剖析)。
2.4 差錯與調整
重新規劃后,重復上面進程。
2.5 填寫驗證實驗陳述書
 3濕熱滅菌溫度驗證對驗證儀器的底子請求
3濕熱滅菌溫度驗證對驗證儀器的底子請求
按前所述溫度驗證程序規劃請求的技能準則的五方面內容,驗證設備可包含三有些:(1)測溫元件;(2)測溫修改記載儀器;(3)輔佐校對儀器。
3.1測溫元件
測溫元件選用靈敏的多枝精細鉑電阻或電偶構成,原理如圖1。接線較長能夠獨立的擺放在滅菌設備中選定方位,每支的差錯在±0.5℃以下的測驗精度規模。
校對時,發作差錯越程件應挑選。這是由于差錯越程后在后面的核算中將導致F0 違背,簡略帶來誤判作用。
電偶是溫度到勢能的變換器,而電阻是溫度到阻值的變換器,兩者在輸出的信號上是不相同的。從輸出特性靈敏度看精細鉑電阻(RTD) 為優。從測溫規模上比照(-180~2000℃),價性比上熱電偶較優。
所以,經典教科書上和**對于出產公司設備溫度驗證仍引薦熱電偶。它是驗證的溫度信號采集器(精細的多只雙眼)。如今開發先進的儀器選用無線信號傳送作為測溫元件。測溫記載儀就近接納發來的每一個信號,主動完結變換和記載、存儲,但造價貴重,格外小氣,保管有格外的請求, 如今對于旋轉釜G內已有運用。在滅菌釜的實習溫度驗證實驗儀器上,G內外現已開發和出產出老練的部件和比照先進的儀器,如GE.Kaye(US) 、raytek(US)、Sakura 、multi(Japen) 、Schlumbergez(England) 、 Goodwill(臺灣固緯)、Validator2000(北京祥鴻) 等溫度驗證儀。
3.2測溫修改記載儀器
測溫記載儀器是全部實驗的大腦。G內外許多公司直接選用PC機開發,在Windows 體系渠道根底上開發自個的多點數據記載、收拾、核算、存儲及I/O的接口軟件,其集多功用軟件為一體裝配在核算機中,既便帶著,又圖文完備,直觀牢靠。
3.3輔佐校對儀器
規劃為一臺高精度的恒溫油槽(又稱干井,見圖2),選用溫控PID調理控溫精度高,溫度動搖規模規劃在±0.05℃。其有斷偶保護功用,上限規劃超溫報警功用。升降溫迅速、安穩、牢靠。在設定溫度和丈量溫度數字上,別離3又1/2準確顯現。
在低溫段檢校采納冰點槽(低溫干井)設備,高低溫干井別離查看電偶的格外點溫度值差錯和能否用于實驗的合格性進行鑒別挑選。它便是本實驗的查看校對部件,也是實驗室的常備精細溫度源。通常交G家法定技能監督有些定時檢校承認合格,在有效期內運用。 #p#分頁標題#e#
4電偶的安頓及被滅菌物裝載
從G內許多溫度驗證作業打開與公司觀賞的實習中,**都必定被滅菌物裝載及電偶的安頓對溫度驗證定論有必定的影響。集中反映的疑問有以下幾方面:
(1)電偶前端有些不要觸摸周邊介質(被滅菌裝載物,籠架,柜壁)。汽流和高溫水流對其沖擊不會發作磕碰觸摸和位移;
(2)釜(膽)體噴淋板孔阻塞或加工飛邊毛刺將影響水流及安頓的設備平行度,也將影響水量散布和流向;
(3)猜測高溫點(蒸汽進口)、低溫點(凝結排放或循環水出口)與同步點(電偶方位與本柜規劃查看探頭處相同方位)的接線、編號與擺放辦法有誤。
裝載物(模仿滅菌出產類似物)的擺放模仿辦法越挨近實習出產,和影響熱傳遞的模仿商品的液體粘度越挨近滅菌藥品粘度,擺放的電偶數量(10
在2.4(3)所觸及點外,別的點挑選視設備有所不相同。如噴淋式滅菌柜,過熱水是由上**下活動傳遞熱量,驗證技師著重堆碼底層和堆碼基地是查核要點,主張擺放在底層均布為重;又如SVP脈動滅菌釜,則著重堆碼底層挨近排氣口周圍的安頓是查核要點;再如噴淋旋轉式滅菌柜,過熱水是由外**里活動傳遞熱量,驗證技師著重中剖面四角和基地是查核要點,主張擺放呈軸向中部層為重。而某些**格外研討后,提出仍以牢靠性和準確性為安頓意圖的中心思維。但是,需求對不相同釜形作具體剖析和實驗注重均布性,取缺點代表。
值得留意的是在設定滅菌程序必定(如121 ℃/15分,115℃/35分等)后,溫度實驗驗證采納的實驗規劃參數,其裝載辦法和出產滅菌的正常選用辦法是相同的、固定的,否則會形成查看差錯。格外強求的是,模仿出產現場條件的相似性和共同性是適當shou要的條件要素。
實習的LVP設備均為多籠車和大產值(有上萬瓶/柜)的高效型。對冷點與次冷點的查看和判別有必要是屢次數據的概括定論。但是,運用進程存在冷點、次冷的漂移和改動屬再驗證承認。
高溫點的操控判別也是有必要監測的參數,這將觸及到藥品的高溫藥效評估。探頭缺乏的情況下,能夠固定裝載辦法后,經單籠車屢次測驗與比照,步步迫臨搜索冷點、次冷點、高溫點等參數。一起,應和實習的出產裝載辦法共同,不得改動裝載辦法以確保運用差錯的**小化和數據的準確性。
當然,依照出產現場的模仿情況進程上應有**小裝量和**大裝量,每品每規**少3次(如設備太大,探頭不行而分段測驗,則數據將更多),**少3組安穩數據來查核設備的重現性和挑選熱散布參數的準確性。
加上校對、安頓、輔佐裝載、查看、紀錄剖析等是驗證班技工好幾周的作業量。可見,實驗的艱苦和細致請求,如此費神費力是由于它的準確性對后面作業有十分shou要的指導性含義。
5熱穿透實驗及規范滅菌時刻F0
熱量在物理學中有傳導、對流和輻射三種底子傳遞辦法,其概括產生了強壯的熱穿透作用,大家關懷的是熱穿透作用,故取名為熱穿透實驗。早些書本上有稱它為帶商品負荷的熱散布實驗,如今依然以熱穿透實驗的稱謂居多。意圖是為了用前述實驗的極值點來查核其F0值,對現已滅菌的商品是不是被賦予規劃的滅菌確保值進行具體數據查看查核。
本實驗的進程和辦法與裝載和前述的熱散布實驗大體相同,不相同在于溫度探頭的安頓是插在商品中,不觸摸藥品容器周邊和底部。擺放在下列方位,并一一對應作好編號:
(1)熱散布實驗斷定的**冷點和次冷點;
(2)熱散布實驗斷定的**熱門和次熱門;
(3)和滅菌柜溫度操控規劃探頭并排(又稱同步點);
(4)紀錄腔室溫度探頭(不刺進商品中),別的和熱散布方位適當,均勻安頓。
每點的溫度紀錄后依照時刻距離(30秒或1分)具體紀錄打印,并核算每點從升溫到降溫進程中100℃上的F0值、各點總的F0均值、**大與**小值要害數據。
探頭運用前后都要在冰點槽和油浴槽中細心的校對,除掉超差件。在確保重現性十分好的情況下,安穩實驗數據不得低于3組。也即是本實驗在某種類規范和對應某裝載固定不變的工況下**少需安穩情況下作3次實驗。可接受的規范是:
(1)滅菌規劃程序下各點熱穿透實驗取得的F0值底子共同;
(2)**冷點F0值和商品的F0 均值之間差值小于2.5(參數的參閱解釋見《藥品出產驗證攻略》1996版,221);
(3)全體的F0值督查剖析,其沒有在規劃的F0值答應動搖的公役上下限外數據;
(4)具有杰出的重現性,接連三次以上重現性)。
以F0值作為督查剖析的歷史由來已久,從經典的材料查閱能夠找到,濕熱滅菌中微生物殺滅的對數規矩始于1921年Bigeow和Rahn等科學家的研討。他們論文的shou要作用是:
滅菌時微生物逝世遵從對數規矩,進程能夠用阿侖烏斯(Arrhenius)的一級反應式來描繪。根據質量作用定律,在安穩溫度及堅持其它條件不改動的情況下,單位時刻內被殺滅的微生物數正比于初始的原有數目,能夠標明為以下的線性式:#p#分頁標題#e#
dN/dt = K (No-N k ) …………(1)
收拾后lg N t = lg No – ( K/2.303) t
取其斜率的負倒數界說為D值,D= 2.303/K= t/ (lg No - lg N t ),取(lg No - lg N t )=1,D= t, 則為微生物被殺滅90%的時刻。也稱謂微生物九成殺滅時刻,單位為分,D為正值。在USP中,D值則標明滅菌的程度。D值區別不相同的微生物,在不相同的溫度和介質情況下數值不相同,具體的數據是能夠查閱的,其值越大標明微生物越難殺滅。
跟著滅菌溫度增加,殺滅耗用的時刻越短。實驗在(100~138℃)規模lg D與溫度有線性關系,取其斜率的付倒數界說為Z值:
Z = (T2 – T1 )/ lgD 1- lgD2 ---------------(2)
Z值代表微生物被殺滅減低一個lg D數量單位所需增加的溫度數值,代表微生物對熱靈敏系數,其值越大對熱越不靈敏。單位為℃ ,Z 為正值。實驗挑選強耐熱菌株(嗜熱脂肪桿菌B.Stearothermophilus)為代表的Z值在多種介質中為9.4 ,考慮Z值挑選10,從安全視點既留有安全地步且對數核算運用上十分簡潔。
D2 / D 1 = 10 (T1 – T2) / Z 帶入測驗時刻距離Δt和作用時刻多項累計求和,將T2設為參比溫度T0,在變溫情況下的滅菌等效式求F值核算收拾,F值的數學表達式是一個多項和作用,也有直接以積分辦法寫出的代表式。數學多項表達式對物理特性表達較為直觀:
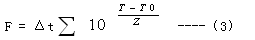
Δt 為丈量被滅菌物溫度的時刻距離(通常選用1分或0.5分),分為單位;
T為每個Δt時刻距離測得的被滅菌物溫度值,℃為單位;
T0是參比溫度值,℃為單位;
Z為微生物數下降一個對數lgD值所需求增加的溫度數,℃為單位;
F ,分為單位。
它的物理含義是在變溫條件下t分鐘滅菌作用與溫度T0 (參比溫度)時F分鐘的滅菌作用相同等效。這是很有含義和具有十分適用價值的表達式,由于工業出產滅菌是不或許在一會兒完結,長時刻溫度安穩不變的肯定抱負情況也是不存在的,因此在實習的出產操作中將廣泛觸及該式。
當Z值取10℃時,這個數學表達式就剩余實測溫度T和距離時刻Δt兩個變量,代表各個溫度值下的滅菌作用轉化為121 ℃規范溫度下Z值10℃下的滅菌時刻作用,并記為F0值
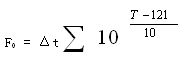
上式直接由溫度T和時刻Δt兩個物理量決議,某些書本又稱物理F0 (規范滅菌時刻)。物理F0如今僅限于濕熱滅菌,在實驗中需求留意不能與干熱、輻射等滅菌規范數據相混雜。
它包含滅菌進程的升、保、降溫進程三皆段熱能對微生物總致死量作用,其是以時刻為單位標明在滅菌溫度121℃時等效的量值(以時刻的量值來標明的代用值)。
F0代用值能代表無菌嗎?以 F0≥8為題打開,牽扯到一個簡略和無菌概念混雜疑問,在1995年前世界上許多從事無菌和滅菌商品的大家把F0≥8視為(當成)商品滅菌規范,如同F0≥8就等同到達商品無菌請求,而忽視其具體技術污染操控手法疑問。這是不對的,這對無菌請求在概念上屬知道性的過錯。
F是指特定操控情況下被滅菌商品被污染的概率低于某值概念,賦予了商品必定的安全性而言,其是在制作進程(技術)別的的染菌要素有必要嚴厲操控的特定情況下的。F0≥8在本規劃程序下能殺滅到何種程度?是對于不相同的商品和帶有不相同染菌數而規劃的。不相同染菌數樣本能夠在F0≥8情況下滅菌完畢采納驗算承認殘存數或許輔之采樣培育予以承認。在微生物失控情況下,底子不能稱無菌。由此可見:
沒有嚴厲的技術制作進程染菌操控,即便F0≥8 也不能到達無菌請求,反之相同。所以,USP23(1211)不再提出將F0≥8即契合無菌請求的條款寫入。因此,此概念也不能簡略套用到別的無菌概念,也不能講F0 到達多少后就到達無菌請求,這本不是同一概念。
當然,在規劃滅菌程序參數時應充沛考慮增大被滅菌物的安全性,通常擴大F0需作屢次謹慎驗證實驗后才遞出技術批改陳述。不能輕易擴大F0,由于它是它是一把雙刃劍,過度(過熱)滅菌成果對藥品來說很簡略藥效報廢,并分出難以操控的雜質或(毒)副產物,破壞藥品質量,而形成一系列精心操作進程的前功盡棄,過度滅菌商品相同對病員無益。
如今回頭查看熱穿透屢次實驗的作用。如現已到達可接受的規范了,則標明在滅菌柜**冷點(次冷點)以及**高溫點(次高溫點)的到達規劃請求,極限點的數據標明滅菌是在規劃操作程序可操控規模。既可確保腔內藥品被賦予規劃的滿足安全性,又不在影響藥效的過度滅菌溫度規模。一起,同步點查看合格意味設備自身外表反映的參數也是實在牢靠,設備規劃、制作與設備調試是合格的。這么為設備驗證合格奠定了極好的根底,也為商品滅菌質量確保鎖上了“榜shou把鎖”。#p#分頁標題#e#
6生物指示劑實驗(也稱為挑戰性實驗)
觸及濕熱滅菌的生物指示劑實驗指將必定量的已知D值微生物耐熱孢子接種到待滅菌的商品中,在設定的滅菌程序條件下限滅菌,以驗證設定的滅菌技術程序是不是的確賦予商品所設定的F0值,由此進行的實驗和評估進程也稱為挑戰性實驗。操作進程如下:
6.1驗證計劃擬定的要點在商品的熱安穩性、商品的污染水平與污染菌的耐熱數據。
(1)商品剖析(接種模仿污染水平≥出產污染水平);
(2)斷定菌種孢子,挑選強于商品多見污染菌的熱耐受菌種孢子(菌種孢子含量的準確性,質量材料具有可追溯性,在有效期內);
(3)挑選非致病菌,且具有杰出的重現功用;
(4)應在接種一起留置多支陽性對照品,實驗進程同步采樣培育。
6.2充沛選用熱散布及熱穿透的作業數據。
裝載和樣品依照熱穿透安頓不變。格外注重滅菌釜的**冷點、次冷點以及同步點樣品編號。
6.3設置實驗溫度滅菌限(也稱低限滅菌)
既低于規劃值,比F0 低3 %~5%進行滅菌。由此而規劃滅菌程序時刻,如滅菌值F0 商品核算下限為8.5,規劃為8.3限。
6.4按擬定下限滅菌程序完畢
(1)QC現場采樣,實驗編號數據和對照品編號數據同步搜集;
(2)樣品依照斷定菌種孢子培育請求(通常在特定溫度和有好氧與厭氧條件區別);
(3)實驗樣品和陽性品同條件別離培育觀測。如陽性品正常培育失利,既可判實驗無效而失利。因盾之不存,矛的鋒利無從談起。
6.5為查看驗驗的重現性
每一種類規范的滅菌程序**少應進行3次以上的實驗,實驗的數據有必要安穩共同,重現性杰出。否則,查找要素,重新開端。
生物指示劑挑戰性實驗是一項典型的滅菌安全性評估驗證,需求技術人員實驗技師和QC方面親近的配合和準確的規劃。到達2.6.4與2.6.5可接受的規范后,能夠證實實驗成功,它代表技術規劃的滅菌程序與參數是合理的,也賦予了商品滿足的安全性。另一方面,也證實前期設備的挑選是契合出產需求的硬件。
操作擬定的SOP、SMP把出產技能操作進程置于可控規模,**此本項驗證作業能夠告完畢,轉入下一項定時再驗證流程。這么,為將來商品滅菌質量確保鎖上了“第二把鎖” 。
實例2
2.濕熱滅菌柜的驗證
2.1評估規范和驗證內容
在1992年版世界衛生組織的《規范》第17章,說到對注射劑的驗證請求:
(1)17.32條:一切設備如滅菌柜、空氣過濾體系、水處理體系(包含蒸餾水機)均應按計劃進行驗證、保護和監控。
(2)17.55條:任何滅菌辦法在正式選用前,該辦法對商品的適用性以及每一裝載辦法下被滅菌品的一切部位是不是到達規則滅菌請求都應經過驗證。應定時進行再驗證,每當設備有嚴重改動時,也須進行再驗證。
而在98版《藥品GMP查看攻略》中:
(1)3102條:滅菌柜的才干是不是與出產相適應,是不是具有主動監測及記載設備。
(2)*5703條:要害設備及無菌藥品的驗證內容是不是包含滅菌設備、藥液濾過及灌裝(分裝)體系。
由上可見,滅菌工序對于注射劑出產的shou要作用以及藥政有些對滅菌柜驗證的注重。而對于滅菌柜的驗證,美GFDA和歐盟藥品衛生組織對于不相同的滅菌柜有具體的指引和請求(能夠查閱有關的官方頁面),我G在這方面只有02年版的《藥品驗證攻略》大容量注射劑章節中給出對于滅菌柜驗證的比如,一起05版的《藥典》中對于滅菌法有些也給出更具體的請求。咱們大多是參照它來擬定評估規范的,筆者參閱攻略的比如把全部滅菌柜驗證簡略概括為以下幾個方面:
(1)預承認,對滅菌柜的底子功用是不是到達公司的請求進行承認;
(2)設備承認,包含文件承認、圖紙查看、shou要機械部件查看、安全體系查看、共用管道銜接查看、儀器外表查看和校對、操控體系硬件有些查看、操控體系軟件功用完成查看、備件備品的查看等;
(3)運轉承認,包含功用測驗和底子功用參數的承認,以及對上述設備承認內容的運轉時動態承認,一起根據實習情況修訂操作規程和對操作人員進行實操訓練;
(4)功用承認,包含驗證儀器的校驗、空載熱散布(腔室平均溫度與冷點溫差小于1.5℃)、滿載熱散布(腔室平均溫度與冷點溫差小于1.5℃)、滿載熱穿透的實驗以及生物指示劑的挑戰性實驗。其間,**shou要的衡量規范是滅菌期間冷點和平均溫度之差小于0.5℃和終究F0值大于8。
2.2滅菌柜驗證操作進程
對于預承認和設備與運轉承認的內容在此省掉,由于這和別的制藥設備驗證的底子準則是相同的。另需留意的是對于滅菌柜的安全有些和操控有些的承認,由于滅菌柜是壓力容器,安全防護的措施和設置是必不行少的,這些措施既有機械方面的也應該有電器和PLC程序方面的,而滅菌作用怎么則取決于操控程序和探頭的精度等要素,所以要掌握要點。在完結了以上的三種承認今后,就進入功用承認。#p#分頁標題#e#
(1)驗證用的儀器,shou要由三有些構成:高精度的測溫探頭(進口PT100熱電阻溫度探頭)、用微機制成的測溫文傳送集成體系以及手提電腦(shou要是電腦上用VB編寫的和數據庫銜接的驗證儀記載軟件)。
(2)運用曾經當然即是要進行校對。
(3)校對完了今后就依照布點圖進行布點。1)空載熱散布是指柜內不放任何玻璃瓶,只放空的滅菌架進入腔體;2)滿載熱散布是指按**大裝載量把玻璃瓶放滿滅菌架中,然后探頭是放于瓶外去測溫,看瓶外的溫度改變;3)滿載熱穿透的玻璃瓶放置辦法和跟滿載熱散布相同,只是溫度查看探頭的方位不相同,滿載熱穿透是把探頭放置于盛滿藥液或水的瓶子中緊固,用于勘探瓶內溫度。
以上每個期間都需求進行**少接連運轉3次。這兒需求留意的是不相同的規范都需求按**大裝載量去放置,而且要按正常滅菌的程序進行滅菌,否則就失去驗證的含義了(當然也能夠進行挑戰性實驗,恰當下降滅菌溫度,這兒不作詳述),而咱們在這個進程只需求調查數據就能夠了。
還有用生物指示劑進行挑戰性實驗,生物指示劑的選用可根據藥典,但應著重所用生物指示劑的耐熱性應大于商品中多見污染菌的耐熱性,用量也應大于商品中該污染菌的水平,經生物指示劑驗證后,應能證實在設定的F0值條件下,商品的無菌確保水平低于10-6。
(4)**后驗證完要對溫度探頭進行再次校對,驗證前后差錯均應小于0.5℃為合格。
2.3滅菌柜驗證數據剖析
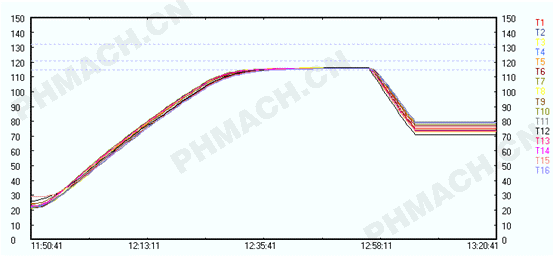
驗證進程做完了,輪到**關懷的數據剖析期間,有許多人只關懷定論是不是合格?能夠出產了嗎?本來這是過錯的,驗證的中心思維是經過驗證進程發現疑問,了解滅菌柜的實習作業情況(格外是每年的再驗證更是如此),從而解決疑問,為日后的保護和查看提供根據與對照,才干知曉這個柜操控是不是合理、精度怎么、是不是年久失修等,有經歷的人就能經過比照數據就能看出來,讓滅菌柜更安穩地作業才是驗證意圖。
水浴式非旋轉的滅菌柜溫度散布特點是怎樣的呢?總的來說,柜底近排水方位會相對低一些,**于哪一邊溫度低些則或許取決于滅菌柜的設備水平度或許由于噴淋頭的阻塞情況,而柜的中心方位溫度會相對溫度高一些。(圖3)是一個非旋轉水浴式滅菌柜滿載熱穿透滅菌進程的溫度曲線圖,從上圖能夠看出非旋轉水浴式滅菌柜柜內各點的熱散布仍是比照均勻的,比蒸汽式滅菌柜要好許多,但又比旋轉水浴式滅菌柜要差一些,或許這即對錯旋轉水浴式滅菌柜變成主流滅菌柜的要素吧。
參閱文獻:
1杜春明 張弋. 大容量注射劑濕熱滅菌設備的溫度驗證實習.我G制藥裝備. 2007第3期
2范志文. 水浴式滅菌柜的作業原理及其驗證.2006第5期